ааЕбаЕаГббаПаПаИбаОаВаКаА аЄаАаВаОббаКаОаГаО — аПаЕбаЕаГббаПаПаИбаОаВаКаА ЮБ-аГаАаЛаОаГаЕаНаКаЕбаОаНаОаВ (б аЛаОбаО- , аБбаОаМаО- аИаЛаИ аИаОаД-) аВ аКаАбаБаОаНаОаВбаЕ аКаИбаЛаОбб аИаЛаИ аИб аПбаОаИаЗаВаОаДаНбаЕ (ббаИбб аИаЛаИ аАаМаИаДб) аПаОаД аДаЕаЙббаВаИаЕаМТ аОбаНаОаВаАаНаИаЙ.
абаОаДбаКб баЕаАаКбаИаИ аЗаАаВаИбаИб аОб аПбаИбаОаДб аОбаНаОаВаАаНаИб: аВ баЛббаАаЕ аГаИаДбаОаКбаИаДаОаВ баЕаЛаОбаНбб аМаЕбаАаЛаЛаОаВ аОаБбаАаЗббббб аКаАбаБаОаНаОаВбаЕ аКаИбаЛаОбб, аПбаИ аВаЗаАаИаМаОаДаЕаЙббаВаИаИ б аАаЛаКаОаГаОаЛббаАаМаИ — баЛаОаЖаНбаЕ ббаИбб, аВ баЛббаАаЕ аАаМаИаНаОаВ — аАаМаИаДб аКаАбаБаОаНаОаВбб аКаИбаЛаОб.
ааЕбаЕаГббаПаПаИбаОаВаКаА аАаЛаИбаИаКаЛаИбаЕбаКаИб аГаАаЛаОаГаЕаНаКаЕбаОаНаОаВ баОаПбаОаВаОаЖаДаАаЕббб ббаЖаЕаНаИаЕаМ баИаКаЛаА.
абаИаМаЕбаОаМ баЕаАаКбаИаИ аМаОаЖаЕб баЛбаЖаИбб аОаБбаАаЗаОаВаАаНаИаЕ баИаКаЛаОаПаЕаНбаАаН-аКаАбаБаОаНаОаВаОаЙТ аКаИбаЛаОббТ аИаЗ 2-б аЛаОббаИаКаЛаОаГаЕаКбаАаНаОаНаА аПаОаД аДаЕаЙббаВаИаЕаМ аАаЛаКаОаГаОаЛббаАТ аКаАаЛаИб:

ааБббаНаО аГаАаЛаОаГаЕаНаКаЕбаОаН баМаЕбаИаВаАбб б аКаОаНбаЕаНббаИбаОаВаАаНаНбаМ баАббаВаОбаОаМТ аОбаНаОаВаАаНаИбТ (аНаАаПбаИаМаЕб, аВТ баПаИббаЕ) аИаЛаИ бТ бббаПаЕаНаЗаИаЕаЙТ аОбаНаОаВаАаНаИбТ аВ баАббаВаОбаИбаЕаЛаЕ (ббаАаНаОаЛаЕ, ббаИбаЕ,Т баОаЛбаОаЛаЕ) аПбаИ баЕаМаПаЕбаАбббаЕ аОб -20 аДаО +300C. а аЕаАаКбаИаОаНаНаАб баМаЕбб аВбаДаЕбаЖаИаВаАбб 10-30 аМаИаН (аВ баЛббаАаЕ аНаИаЗаКаОбаЕаАаКбаИаОаНаНаО-баПаОбаОаБаНбб аКаЕбаОаНаОаВ — 2-4 б аПбаИ аНаАаГбаЕаВаАаНаИаИ).
а аКаАбаЕббаВаЕ аОбаНаОаВаАаНаИаЙ аПбаИаМаЕаНббб аГаИаДбаОаОаКаИбаИ баЕаЛаОбаНбб аИаЛаИ баЕаЛаОбаНаО-аЗаЕаМаЕаЛбаНбб аМаЕбаАаЛаЛаОаВ, аАаЛаКаОаГаОаЛббб баПаИббаОаВ, аА баАаКаЖаЕ аКаАбаБаОаНаАбб аИаЛаИ аБаИаКаАбаБаОаНаАбб баЕаЛаОбаНбб аМаЕбаАаЛаЛаОаВ, аАаМаМаИаАаК аИаЛаИ аАаМаИаНб.
а аЕТаАаКТбаИб аИбТаПаОаЛбТаЗбТбб аДаЛб баИаНТбаЕТаЗаА аЗаАТаМаЕТбаЕаНТаНбб аКаАбТаБаОТаНаОТаВбб аКаИТбаЛаОб, баИаКаЛаИбаЕбаКаИб аКаЕбаОаНаОаВ, аВ баИаНТбаЕТаЗаЕ ббаЕТбаОаИТаДаОаВ, аАаМаИаНаОаВ аИаЛаИ баЛаОаЖаНбб ббаИбаОаВ
а аЕаАаКбаИб аОбаКбббаА A. E. аЄаАаВаОббаКаИаМ аВ 1894 аГ.
ааЕб аАаНаИаЗаМ баЕаАаКбаИаИ
аЁббаЕббаВбаЕб аДаВаЕ аВаОаЗаМаОаЖаНаОббаИ аПбаОбаЕаКаАаНаИб баЕаАаКбаИаИ, аКаОбаОббаЕ аОбббаЕббаВаЛббббб аВ аЗаАаВаИбаИаМаОббаИ аОб аЗаАаМаЕббаИбаЕаЛаЕаЙ.
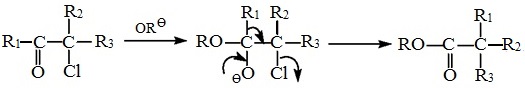
а аКаЛаАббаИбаЕбаКаОаМ аВаАбаИаАаНбаЕ аПаЕбаЕаГббаПаПаИбаОаВаКаИ баАаДаИаКаАаЛ R баОаДаЕбаЖаИб аАбаОаМ аВаОаДаОбаОаДаА б ЮБ-аАбаОаМаА баГаЛаЕбаОаДаА. а аОббббббаВаИаЕ ЮБ-аВаОаДаОбаОаДаНаОаГаО аАбаОаМаА баЕаАаКбаИб аОаБббаНаО аИаДаЕб аВ ббаАаВаНаИбаЕаЛбаНаО аЖаЕббаКаИб ббаЛаОаВаИбб (аНаАаПбаИаМаЕб, аПбаИ аКаИаПббаЕаНаИаИ б NaOH аВ баОаЛбаОаЛаЕ) аИ аНаАаЗбаВаАаЕббб аКаВаАаЗаИаПаЕбаЕаГббаПаПаИбаОаВаКаОаЙ аЄаАаВаОббаКаОаГаО.
ааЕб аАаНаИаЗаМ аКаЛаАббаИбаЕбаКаОаЙ аПаЕбаЕаГббаПаПаИбаОаВаКаИ аВаКаЛббаАаЕб аОаБбаАаЗаОаВаАаНаИаЕ аНаА аПбаОаМаЕаЖббаОбаНаОаЙ ббаАаДаИаИ баИаКаЛаОаПбаОаПаАаНаОаНаА. ааОаД аДаЕаЙббаВаИаЕаМ аГаИаДбаОаКбаИаЛбаНаОаГаО аИаОаНаА аКаОаЛббаО баИаКаЛаОаПбаОаПаАаНаОаНаА баАбаКббаВаАаЕббб, аПбаОаИбб аОаДаИб аПаЕбаЕаНаОб аПбаОбаОаНаА аИ аОаБбаАаЗбаЕббб аКаОаНаЕбаНбаЙ аПбаОаДбаКб. аІаИаКаЛаОаПбаОаПаАаНаОаНб аВаО аМаНаОаГаИб баЛббаАбб баДаАаЕббб аВбаДаЕаЛаИбб.
абаИ аНаАаЛаИбаИаЕ аЕаНаОаЛаИаЗаИббаЕаМаОаГаО аАбаОаМаА аВаОаДаОбаОаДаА аВ аИбб аОаДаНаОаМ аГаАаЛаОаГаЕаНаКаЕбаОаНаЕ аПбаОаИбб аОаДаИб аЕаГаО аДаЕаПбаОбаОаНаИбаОаВаАаНаИаЕ, б аОаБбаАаЗаОаВаАаНаИаЕаМ аЕаНаОаЛббаА, аКаОбаОббаЙ аВаНбббаИаМаОаЛаЕаКбаЛббаНаО баИаКаЛаИаЗбаЕббб б аОаБбаАаЗаОаВаАаНаИаЕаМ аПбаОаМаЕаЖббаОбаНаОаГаО баИаКаЛаОаПбаОаПаАаНаКаЕбаОаНаА.
ааЕбаОаГббаПаПаА баИаКаЛаОаПбаОаПаАаНаКаЕбаОаНаА аПаОаДаВаЕбаГаАаЕббб аНбаКаЛаЕаОбаИаЛбаНаОаЙ аАбаАаКаЕ аАаЛаКаОаГаОаЛббаОаМ (аИаЛаИ аГаИаДбаОаКбаИаЛаОаМ) б аОаБбаАаЗаОаВаАаНаИаЕаМ баЛаЕаДбббаЕаГаО баОаЕаДаИаНаЕаНаИб, ббаО аПбаИаВаОаДаИб аК баАбаКбббаИб баИаКаЛаОаПбаОаПаАаНаОаВаОаГаО ббаАаГаМаЕаНбаА б аОаБбаАаЗаОаВаАаНаИаЕаМ аКаАбаБаАаНаИаОаНаА. ааАаЛбаНаЕаЙбаЕаЕ аПбаОбаОаНаИбаОаВаАаНаИаЕ аДаАаЕб аКаОаНаЕбаНбаЙ аПбаОаДбаКб баЕаАаКбаИаИ.


ааВаАаЗаИаПаЕбаЕаГббаПаПаИбаОаВаКаА аЄаАаВаОббаКаОаГаО аПбаОбаЕаКаАаЕб аПаО баАаК аНаАаЗбаВаАаЕаМаОаМб баЕаМаИаБаЕаНаЗаИаЛбаНаОаМб аМаЕб аАаНаИаЗаМб. а ббб аПаЕбаЕаГббаПаПаИбаОаВаКб аВбббаПаАбб ЮБ-аГаАаЛаОаГаЕаНаКаЕбаОаНб, аНаЕ аИаМаЕббаИаЕ аВаОаДаОбаОаДаНбб аАбаОаМаОаВ аВ ЮБ -аПаОаЛаОаЖаЕаНаИаИ аК аКаАбаБаОаНаИаЛбаНаОаЙ аГббаПаПаЕ аЁ=O.
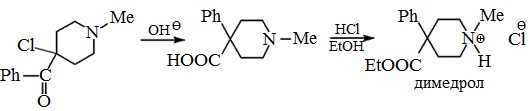
абаИаМаЕбаОаМ баАаКаОаЙ баЕаАаКбаИаИ аМаОаЖаЕб баЛбаЖаИбб аПаОаЛббаЕаНаИаЕ аПбаЕаПаАбаАбаА аДаЕаМаЕбаОаЛаА:

 а баБбаИаКаИ:
а баБбаИаКаИ: 