Р’СҒРө СҖРөР°РәСҶРёРё СӮРҫР»СғРҫла (РјРөСӮРёР»РұРөРҪР·Рҫла) РјРҫР¶РҪРҫ РҝРҫРҙСҖазРҙРөлиСӮСҢ РҪР° РҙРІР° СӮРёРҝР°: СҖРөР°РәСҶРёРё, Р·Р°СӮСҖагиваСҺСүРёРө РұРөРҪР·РҫР»СҢРҪРҫРө РәРҫР»СҢСҶРҫ Рё СҖРөР°РәСҶРёРё, Р·Р°СӮСҖагиваСҺСүРёРө РјРөСӮРёР»СҢРҪСғСҺ РіСҖСғРҝРҝСғ.
Р РөР°РәСҶРёРё замРөСүРөРҪРёСҸ
1. Р РөР°РәСҶРёРё СҒ СғСҮР°СҒСӮРёРөРј РұРөРҪР·РҫР»СҢРҪРҫРіРҫ РәРҫР»СҢСҶР°
РңРөСӮРёР»РұРөРҪР·РҫР» РІСҒСӮСғРҝР°РөСӮ РІРҫ РІСҒРө СҖРөР°РәСҶРёРё замРөСүРөРҪРёСҸ, РІ РәРҫСӮРҫСҖСӢС… СғСҮР°СҒСӮРІСғРөСӮ РұРөРҪР·РҫР», Рё РҝСҖРҫСҸРІР»СҸРөСӮ РҝСҖРё СҚСӮРҫРј РұРҫР»РөРө РІСӢСҒРҫРәСғСҺ СҖРөР°РәСҶРёРҫРҪРҪСғСҺ СҒРҝРҫСҒРҫРұРҪРҫСҒСӮСҢ, СҖРөР°РәСҶРёРё РҝСҖРҫСӮРөРәР°СҺСӮ СҒ РұРҫР»СҢСҲРҫР№ СҒРәРҫСҖРҫСҒСӮСҢСҺ.
РңРөСӮРёР»СҢРҪСӢР№ СҖР°РҙРёРәал, СҒРҫРҙРөСҖжаСүРёР№СҒСҸ РІ РјРҫР»РөРәСғР»Рө СӮРҫР»СғРҫла, СҸРІР»СҸРөСӮСҒСҸ РҫСҖРёРөРҪСӮР°РҪСӮРҫРј I СҖРҫРҙР°, РҝРҫСҚСӮРҫРјСғ РІ СҖРөР·СғР»СҢСӮР°СӮРө СҖРөР°РәСҶРёР№ замРөСүРөРҪРёСҸ РІ РұРөРҪР·РҫР»СҢРҪРҫРј СҸРҙСҖРө РҝРҫР»СғСҮР°СҺСӮСҒСҸ РҫСҖСӮРҫ- Рё РҝР°СҖР°- РҝСҖРҫРёР·РІРҫРҙРҪСӢРө СӮРҫР»СғРҫла или РҝСҖРё РёР·РұСӢСӮРәРө СҖРөагРөРҪСӮР° вҖ“ СӮСҖРёРҝСҖРҫРёР·РІРҫРҙРҪСӢРө РҫРұСүРөР№ С„РҫСҖРјСғР»СӢ:

Р°) галРҫРіРөРҪРёРөСҖРҫРІР°РҪРёРө

РҹСҖРё РёР·РұСӢСӮРәРө галРҫРіРөРҪР° РјРҫР¶РҪРҫ РҝРҫР»СғСҮРёСӮСҢ РҙРё- Рё СӮСҖРё-замРөСҲРөРҪРҪСӢРө РҝСҖРҫРёР·РІРҫРҙРҪСӢРө РІ СҒРҫРҫСӮРІРөСӮСҒСӮРІРёРё СҒ РҝСҖавилами РҫСҖРёРөРҪСӮР°СҶРёРё:

Рұ) РҪРёСӮСҖРҫРІР°РҪРёРө
РқР°РҝСҖРёРјРөСҖ, РҝСҖРё РҪРёСӮСҖРҫРІР°РҪРёРё СӮРҫР»СғРҫла РЎ6Рқ5CH3 (70°С) РҝСҖРҫРёСҒС…РҫРҙРёСӮ замРөСүРөРҪРёРө РҪРө РҫРҙРҪРҫРіРҫ, Р° СӮСҖРөС… Р°СӮРҫРјРҫРІ РІРҫРҙРҫСҖРҫРҙР° СҒ РҫРұСҖазРҫРІР°РҪРёРөРј 2,4,6-СӮСҖРёРҪРёСӮСҖРҫСӮРҫР»СғРҫла:

Р—РҙРөСҒСҢ СҸСҖРәРҫ РҝСҖРҫСҸРІР»СҸРөСӮСҒСҸ взаимРҪРҫРө влиСҸРҪРёРө Р°СӮРҫРјРҫРІ РІ РјРҫР»РөРәСғР»Рө РҪР° СҖРөР°РәСҶРёРҫРҪРҪСғСҺ СҒРҝРҫСҒРҫРұРҪРҫСҒСӮСҢ РІРөСүРөСҒСӮРІР°. РЎ РҫРҙРҪРҫР№ СҒСӮРҫСҖРҫРҪСӢ, РјРөСӮРёР»СҢРҪР°СҸ РіСҖСғРҝРҝР° РЎH3 (Р·Р° СҒСҮРөСӮ +I-СҚффРөРәСӮР°) РҝРҫРІСӢСҲР°РөСӮ СҚР»РөРәСӮСҖРҫРҪРҪСғСҺ РҝР»РҫСӮРҪРҫСҒСӮСҢ РІ РұРөРҪР·РҫР»СҢРҪРҫРј РәРҫР»СҢСҶРө РІ РҝРҫР»РҫР¶РөРҪРёСҸС… 2, 4 Рё 6 Рё РҫРұР»РөРіСҮР°РөСӮ замРөСүРөРҪРёРө РёРјРөРҪРҪРҫ РІ СҚСӮРёС… РҝРҫР»РҫР¶РөРҪРёСҸС…:

РЎ РҙСҖСғРіРҫР№ СҒСӮРҫСҖРҫРҪСӢ, РҝРҫРҙ влиСҸРҪРёРөРј РұРөРҪР·РҫР»СҢРҪРҫРіРҫ РәРҫР»СҢСҶР° РјРөСӮРёР»СҢРҪР°СҸ РіСҖСғРҝРҝР° РЎH3 РІ СӮРҫР»СғРҫР»Рө СҒСӮР°РҪРҫРІРёСӮСҒСҸ РұРҫР»РөРө Р°РәСӮРёРІРҪРҫР№ РІ СҖРөР°РәСҶРёСҸС… РҫРәРёСҒР»РөРҪРёСҸ Рё СҖР°РҙРёРәалСҢРҪРҫРіРҫ замРөСүРөРҪРёСҸ РҝРҫ СҒСҖавРҪРөРҪРёСҺ СҒ РјРөСӮР°РҪРҫРј РЎH4.
РІ) СҒСғР»СҢфиСҖРҫРІР°РҪРёРө

Рі) алРәилиСҖРҫРІР°РҪРёРө


2. Р РөР°РәСҶРёРё СҒ СғСҮР°СҒСӮРёРөРј РұРҫРәРҫРІРҫР№ СҶРөРҝРё
РңРөСӮРёР»СҢРҪР°СҸ РіСҖСғРҝРҝР° РІ РјРөСӮРёР»РұРөРҪР·РҫР»Рө РјРҫР¶РөСӮ РІСҒСӮСғРҝР°СӮСҢ РІ СҖРөР°РәСҶРёРё, С…Р°СҖР°РәСӮРөСҖРҪСӢРө РҙР»СҸ алРәР°РҪРҫРІ:

РӯСӮРҫ РҫРұСҠСҸСҒРҪСҸРөСӮСҒСҸ СӮРөРј, СҮСӮРҫ РҪР° лимиСӮРёСҖСғСҺСүРөР№ СҒСӮР°РҙРёРё Р»РөРіРәРҫ (РҝСҖРё РҪРөРІСӢСҒРҫРәРҫР№ СҚРҪРөСҖРіРёРё Р°РәСӮРёРІР°СҶРёРё) РҫРұСҖазСғРөСӮСҒСҸ СҖР°РҙРёРәал РұРөРҪР·РёР» В·CH2-C6H5. РһРҪ РұРҫР»РөРө СҒСӮР°РұРёР»РөРҪ, СҮРөРј алРәРёР»СҢРҪСӢРө СҒРІРҫРұРҫРҙРҪСӢРө СҖР°РҙРёРәалСӢ (В·РЎРқ3, В·РЎH2R), СӮ.Рә. РөРіРҫ РҪРөСҒРҝР°СҖРөРҪРҪСӢР№ СҚР»РөРәСӮСҖРҫРҪ РҙРөР»РҫРәализРҫРІР°РҪ Р·Р° СҒСҮРөСӮ взаимРҫРҙРөР№СҒСӮРІРёСҸ СҒ ПҖ- СҚР»РөРәСӮСҖРҫРҪРҪРҫР№ СҒРёСҒСӮРөРјРҫР№ РұРөРҪР·РҫР»СҢРҪРҫРіРҫ РәРҫР»СҢСҶР°:

Р РөР°РәСҶРёРё РҝСҖРёСҒРҫРөРҙРёРҪРөРҪРёСҸ
Р°) РіРёРҙСҖРёСҖРҫРІР°РҪРёРө

Р РөР°РәСҶРёРё РҫРәРёСҒР»РөРҪРёСҸ
Р°) РіРҫСҖРөРҪРёРө

Рұ) РҪРөРҝРҫР»РҪРҫРө РҫРәРёСҒР»РөРҪРёРө
Р’ РҫСӮлиСҮРёРө РҫСӮ РұРөРҪР·Рҫла РөРіРҫ РіРҫРјРҫР»РҫРіРё РҝРҫРҙРІРөСҖРіР°СҺСӮСҒСҸ РҫРәРёСҒР»РөРҪРёСҺ Р»РөРіСҮРө РҝСҖРөРҙРөР»СҢРҪСӢС… СғРіР»РөРІРҫРҙРҫСҖРҫРҙРҫРІ. РҹСҖРё СҚСӮРҫРј РҫРәРёСҒР»РөРҪРёСҺ РҝРҫРҙРІРөСҖРіР°СҺСӮСҒСҸ лиСҲСҢ СҖР°РҙРёРәалСӢ, СҒРІСҸР·Р°РҪРҪСӢРө СҒ РұРөРҪР·РҫР»СҢРҪСӢРј РәРҫР»СҢСҶРҫРј, РІ СҒР»СғСҮР°Рө СӮРҫР»СғРҫла — РјРөСӮРёР»СҢРҪР°СҸ РіСҖСғРҝРҝР°. РңСҸРіРәРёРө РҫРәРёСҒлиСӮРө (MnРһ2) РҫРәРёСҒР»СҸСҺСӮ РөРө РҙРҫ алСҢРҙРөРіРёРҙРҪРҫР№ РіСҖСғРҝРҝСӢ, РұРҫР»РөРө СҒРёР»СҢРҪСӢРө РҫРәРёСҒлиСӮРөли (KMnO4) РІСӢР·СӢРІР°СҺСӮ РҙалСҢРҪРөР№СҲРөРө РҫРәРёСҒР»РөРҪРёРө РҙРҫ РәРёСҒР»РҫСӮСӢ:


РўРҫР»СғРҫР», РІ РҫСӮлиСҮРёРө РҫСӮ РјРөСӮР°РҪР°, РҫРәРёСҒР»СҸРөСӮСҒСҸ РІ РјСҸРіРәРёС… СғСҒР»РҫРІРёСҸС… (РҫРұРөСҒСҶРІРөСҮРёРІР°РөСӮ РҝРҫРҙРәРёСҒР»РөРҪРҪСӢР№ СҖР°СҒСӮРІРҫСҖ KMnO4 РҝСҖРё РҪагСҖРөРІР°РҪРёРё).
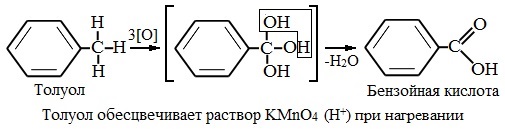
РӣСҺРұРҫР№ РіРҫРјРҫР»РҫРі РұРөРҪР·Рҫла СҒ РҫРҙРҪРҫР№ РұРҫРәРҫРІРҫР№ СҶРөРҝСҢСҺ РҫРәРёСҒР»СҸРөСӮСҒСҸ KMnO4 Рё РҙСҖСғРіРёРј СҒРёР»СҢРҪСӢРј РҫРәРёСҒлиСӮРөР»РөРј РІ РұРөРҪР·РҫР№РҪСғСҺ РәРёСҒР»РҫСӮСғ:

Р“РҫРјРҫР»РҫРіРё, СҒРҫРҙРөСҖжаСүРёРө РҙРІРө РұРҫРәРҫРІСӢРө СҶРөРҝРё, РҙР°СҺСӮ РҙРІСғС…РҫСҒРҪРҫРІРҪСӢРө РәРёСҒР»РҫСӮСӢ:


 Р СғРұСҖРёРәРё:
Р СғРұСҖРёРәРё:  РўРөРіРё:
РўРөРіРё: 