ąöą╗čÅ čåąĖą║ą╗ąŠą░ą╗ą║ą░ąĮąŠą▓ čģą░čĆą░ą║č鹥čĆąĮčŗ ą║ą░ą║ čüčéčĆčāą║čéčāčĆąĮą░čÅ, čéą░ą║ ąĖ ą┐čĆąŠčüčéčĆą░ąĮčüčéą▓ąĄąĮąĮą░čÅ ąĖąĘąŠą╝ąĄčĆąĖčÅ.
ąĪčéčĆčāą║čéčāčĆąĮą░čÅ ąĖąĘąŠą╝ąĄčĆąĖčÅ
1. ąśąĘąŠą╝ąĄčĆąĖčÅ čāą│ą╗ąĄčĆąŠą┤ąĮąŠą│ąŠ čüą║ąĄą╗ąĄčéą░:
ą░) ą║ąŠą╗čīčåą░

ą▒) ą▒ąŠą║ąŠą▓čŗčģ čåąĄą┐ąĄą╣

2. ąśąĘąŠą╝ąĄčĆąĖčÅ ą┐ąŠą╗ąŠąČąĄąĮąĖčÅ ąĘą░ą╝ąĄčüčéąĖč鹥ą╗ąĄą╣ ą▓ ą║ąŠą╗čīčåąĄ:

3. ą£ąĄąČą║ą╗ą░čüčüąŠą▓ą░čÅ ąĖąĘąŠą╝ąĄčĆąĖčÅ čü ą░ą╗ą║ąĄąĮą░ą╝ąĖ:

ą¤čĆąŠčüčéčĆą░ąĮčüčéą▓ąĄąĮąĮą░čÅ ąĖąĘąŠą╝ąĄčĆąĖčÅ
1. ą”ąĖčü-čéčĆą░ąĮčü-ąĖąĘąŠą╝ąĄčĆąĖčÅ, ąŠą▒čāčüą╗ąŠą▓ą╗ąĄąĮąĮą░čÅ čĆą░ąĘą╗ąĖčćąĮčŗą╝ ą▓ąĘą░ąĖą╝ąĮčŗą╝ čĆą░čüą┐ąŠą╗ąŠąČąĄąĮąĖąĄą╝ ą▓ ą┐čĆąŠčüčéčĆą░ąĮčüčéą▓ąĄ ąĘą░ą╝ąĄčüčéąĖč鹥ą╗ąĄą╣ ąŠčéąĮąŠčüąĖč鹥ą╗čīąĮąŠ ą┐ą╗ąŠčüą║ąŠčüčéąĖ čåąĖą║ą╗ą░. ąÆ čåąĖčü-ąĖąĘąŠą╝ąĄčĆą░čģ ąĘą░ą╝ąĄčüčéąĖč鹥ą╗ąĖ ąĮą░čģąŠą┤čÅčéčüčÅ ą┐ąŠ ąŠą┤ąĮčā čüč鹊čĆąŠąĮčā ąŠčé ą┐ą╗ąŠčüą║ąŠčüčéąĖ ą║ąŠą╗čīčåą░, ą▓ čéčĆą░ąĮčü-ąĖąĘąŠą╝ąĄčĆą░čģ ŌĆō ą┐ąŠ čĆą░ąĘąĮčŗąĄ.


2. ą×ą┐čéąĖč湥čüą║ą░čÅ (ąĘąĄčĆą║ą░ą╗čīąĮą░čÅ) ąĖąĘąŠą╝ąĄčĆąĖčÅ ąĮąĄą║ąŠč鹊čĆčŗčģ ą┤ąĖ- (ąĖ ą▒ąŠą╗ąĄąĄ) ąĘą░ą╝ąĄčēąĄąĮąĮčŗčģ čåąĖą║ą╗ąŠą▓.
ąóčĆą░ąĮčü-1,2-ą┤ąĖą╝ąĄčéąĖą╗čåąĖą║ą╗ąŠą┐čĆąŠą┐ą░ąĮ ą╝ąŠąČąĄčé čüčāčēąĄčüčéą▓ąŠą▓ą░čéčī ą▓ ą▓ąĖą┤ąĄ ą┤ą▓čāčģ ąŠą┐čéąĖč湥čüą║ąĖčģ ąĖąĘąŠą╝ąĄčĆąŠą▓, ąŠčéąĮąŠčüčÅčēąĖčģčüčÅ ą┤čĆčāą│ ą║ ą┤čĆčāą│čā ą║ą░ą║ ą┐čĆąĄą┤ą╝ąĄčé ąĖ ąĄą│ąŠ ąĘąĄčĆą║ą░ą╗čīąĮąŠąĄ ąĖąĘąŠą▒čĆą░ąČąĄąĮąĖąĄ.


3. ą¤ąŠą▓ąŠčĆąŠčéąĮą░čÅ (ą║ąŠąĮč乊čĆą╝ą░čåąĖąŠąĮąĮą░čÅ) ąĖąĘąŠą╝ąĄčĆąĖčÅ čåąĖą║ą╗ąŠą░ą╗ą║ą░ąĮąŠą▓. ąÆčüąĄ čåąĖą║ą╗čŗ, ą║čĆąŠą╝ąĄ čåąĖą║ą╗ąŠą┐čĆąŠą┐ą░ąĮą░, ąĖą╝ąĄčÄčé ąĮąĄą┐ą╗ąŠčüą║ąŠąĄ čüčéčĆąŠąĄąĮąĖąĄ, čćč鹊 ąŠą▒čāčüą╗ąŠą▓ą╗ąĄąĮąŠ čüčéčĆąĄą╝ą╗ąĄąĮąĖąĄą╝ ą░č鹊ą╝ąŠą▓ čāą│ą╗ąĄčĆąŠą┤ą░ ą║ ąŠą▒čĆą░ąĘąŠą▓ą░ąĮąĖčÄ ąĮąŠčĆą╝ą░ą╗čīąĮčŗčģ (č鹥čéčĆą░菹┤čĆąĖč湥čüą║ąĖčģ) čāą│ą╗ąŠą▓ ą╝ąĄąČą┤čā čüą▓čÅąĘčÅą╝ąĖ. ąŁč鹊 ą┤ąŠčüčéąĖą│ą░ąĄčéčüčÅ ą┐ąŠą▓ąŠčĆąŠčéą░ą╝ąĖ ą┐ąŠ Žā-čüą▓čÅąĘčÅą╝ ąĪŌĆōąĪ, ą▓čģąŠą┤čÅčēąĖą╝ ą▓ čåąĖą║ą╗.
ą¤čĆąĖ čŹč鹊ą╝ ą▓ąŠąĘąĮąĖą║ą░čÄčé čĆą░ąĘą╗ąĖčćąĮčŗąĄ ą║ąŠąĮč乊čĆą╝ą░čåąĖąĖ (ą┐ąŠą▓ąŠčĆąŠčéąĮčŗąĄ ąĖąĘąŠą╝ąĄčĆčŗ) čü čĆą░ąĘąĮąŠą╣ 菹ĮąĄčĆą│ąĖąĄą╣ ąĖ čćą░čēąĄ čĆąĄą░ą╗ąĖąĘčāčÄčéčüčÅ č鹥 ąĖąĘ ąĮąĖčģ, ą║ąŠč鹊čĆčŗąĄ ąŠą▒ą╗ą░ą┤ą░čÄčé ąĮą░ąĖą╝ąĄąĮčīčłąĄą╣ 菹ĮąĄčĆą│ąĖąĄą╣, čé.ąĄ. ą▒ąŠą╗ąĄąĄ čāčüč鹊ą╣čćąĖą▓čŗąĄ. ąØą░ą┐čĆąĖą╝ąĄčĆ, ą▓ čåąĖą║ą╗ąŠą│ąĄą║čüą░ąĮąĄ ąĮą░ąĖą▒ąŠą╗ąĄąĄ čāčüč鹊ą╣čćąĖą▓ąŠą╣ čÅą▓ą╗čÅąĄčéčüčÅ ą║ąŠąĮč乊čĆą╝ą░čåąĖčÅ ┬½ą║čĆąĄčüą╗ą░┬╗.
ąÜąŠąĮč乊čĆą╝ą░čåąĖąĖ čåąĖą║ą╗ąŠą│ąĄą║čüą░ąĮą░
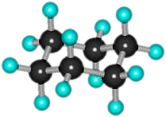
ąÆ čŹč鹊ą╣ ą┐čĆąŠčüčéčĆą░ąĮčüčéą▓ąĄąĮąĮąŠą╣ č乊čĆą╝ąĄ ąŠčéčüčāčéčüčéą▓čāąĄčé čāą│ą╗ąŠą▓ąŠąĄ ąĮą░ą┐čĆčÅąČąĄąĮąĖąĄ, čé.ą║. ą▓čüąĄ ą▓ą░ą╗ąĄąĮčéąĮčŗąĄ čāą│ą╗čŗ ąĖą╝ąĄčÄčé ąĮąŠčĆą╝ą░ą╗čīąĮčŗąĄ ą┤ą╗čÅ sp3-ą│ąĖą▒čĆąĖą┤ąĖąĘąŠą▓ą░ąĮąĮčŗčģ ą░č鹊ą╝ąŠą▓ ąĘąĮą░č湥ąĮąĖčÅ 109┬░28ŌĆÖ.

 ąĀčāą▒čĆąĖą║ąĖ:
ąĀčāą▒čĆąĖą║ąĖ:  ąóąĄą│ąĖ:
ąóąĄą│ąĖ: 