–Ь–µ–Ј–Њ–Љ–µ—А–љ—Л–є —Н—Д—Д–µ–Ї—В (–Ь)¬†вАУ —Н—В–Њ –њ–Њ–ї—П—А–Є–Ј—Г—О—Й–µ–µ –≤–ї–Є—П–љ–Є–µ –∞—В–Њ–Љ–Њ–≤ –Є–ї–Є –≥—А—Г–њ–њ—Л –∞—В–Њ–Љ–Њ–≤, –њ—А–Њ—П–≤–ї—П—О—Й–µ–µ—Б—П –≤ —Б–Љ–µ—Й–µ–љ–Є–Є —Н–ї–µ–Ї—В—А–Њ–љ–Њ–≤ ѕА-¬≠—Б–≤—П–Ј–µ–є –Є–ї–Є –љ–µ–њ–Њ–і–µ–ї–µ–љ–љ—Л—Е —Н–ї–µ–Ї—В—А–Њ–љ–љ—Л—Е –њ–∞—А –Њ—В–і–µ–ї—М–љ—Л—Е –Њ—В–і–µ–ї—М–љ—Л—Е –∞—В–Њ–Љ–Њ–≤ (–Ю, S, N) –≤ —Б—В–Њ—А–Њ–љ—Г –∞—В–Њ–Љ–Њ–≤ —Б –љ–µ–і–Њ—Б—В—А–Њ–µ–љ–љ–Њ–є –і–Њ –Њ–Ї—В–µ—В–∞ —Н–ї–µ–Ї—В—А–Њ–љ–љ–Њ–є –Њ–±–ї–Њ—З–Ї–Њ–є. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –љ–∞ –њ—А–Њ—В–Є–≤–Њ–њ–Њ–ї–Њ–ґ–љ—Л—Е –Ї–Њ–љ—Ж–∞—Е —Б–Є—Б—В–µ–Љ—Л –њ–Њ—П–≤–ї—П—О—В—Б—П –Њ–і–Є–љ–∞–Ї–Њ–≤—Л–µ –њ–Њ –≤–µ–ї–Є—З–Є–љ–µ, –љ–Њ —А–∞–Ј–љ—Л–µ –њ–Њ –Ј–љ–∞–Ї—Г –Ј–∞—А—П–і—Л.
–Ь–µ–Ј–Њ–Љ–µ—А–љ—Л–є —Н—Д—Д–µ–Ї—В (—Н—Д—Д–µ–Ї—В —Б–Њ–њ—А—П–ґ–µ–љ–Є—П) —Е–∞—А–∞–Ї—В–µ—А–µ–љ –і–ї—П —Б–Њ–µ–і–Є–љ–µ–љ–Є–є —Б —Б–Њ–њ—А—П–ґ–µ–љ–љ—Л–Љ–Є —Б–≤—П–Ј—П–Љ–Є, –≤ –Ї–Њ—В–Њ—А—Л—Е –њ—А–Њ—Б—В—Л–µ —Б–≤—П–Ј–Є —З–µ—А–µ–і—Г—О—В—Б—П —Б –Ї—А–∞—В–љ—Л–Љ–Є —Б–≤—П–Ј—П–Љ–Є –Є–ї–Є (–Є) —Б –∞—В–Њ–Љ–∞–Љ–Є, –Є–Љ–µ—О—Й–Є–Љ–Є –љ–µ–њ–Њ–і–µ–ї–µ–љ–љ—Л–µ —Н–ї–µ–Ї—В—А–Њ–љ–љ—Л–µ –њ–∞—А—Л (–Ю, S, N).
–Ь–µ–Ј–Њ–Љ–µ—А–љ—Л–є —Н—Д—Д–µ–Ї—В –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –ї–Є—И—М –≤ —В–Њ–Љ —Б–ї—Г—З–∞–µ, –Ї–Њ–≥–і–∞ –Ј–∞–Љ–µ—Б—В–Є—В–µ–ї—М –≤–Ї–ї—О—З–µ–љ –≤ —Б–Њ–њ—А—П–ґ–µ–љ–љ—Г—О —Б–Є—Б—В–µ–Љ—Г –Љ–Њ–ї–µ–Ї—Г–ї—Л.
–С–ї–∞–≥–Њ–і–∞—А—П –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В–Є ѕА-—Н–ї–µ–Ї—В—А–Њ–љ–Њ–≤ –Љ–µ–Ј–Њ–Љ–µ—А–љ—Л–є —Н—Д—Д–µ–Ї—В –њ–µ—А–µ–і–∞—С—В—Б—П –њ–Њ —Б–Є—Б—В–µ–Љ–µ —Б–Њ–њ—А—П–ґ—С–љ–љ—Л—Е —Б–≤—П–Ј–µ–є –±–µ–Ј —Н—Д—Д–µ–Ї—В–∞ –Ј–∞—В—Г—Е–∞–љ–Є—П.
–Э–∞–њ—А–∞–≤–ї–µ–љ–Є–µ —Б–Љ–µ—Й–µ–љ–Є—П —Н–ї–µ–Ї—В—А–Њ–љ–љ–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ –Ь-—Н—Д—Д–µ–Ї—В–∞ –Њ–±–Њ–Ј–љ–∞—З–∞–µ—В—Б—П –Є–Ј–Њ–≥–љ—Г—В—Л–Љ–Є —Б—В—А–µ–ї–Ї–∞–Љ–Є.

+–Ь-—Н—Д—Д–µ–Ї—В–Њ–Љ –Њ–±–ї–∞–і–∞—О—В –Ј–∞–Љ–µ—Б—В–Є—В–µ–ї–Є, –Ї–Њ—В–Њ—А—Л–µ —Б–Љ–µ—Й–∞—О—В —Н–ї–µ–Ї—В—А–Њ–љ–љ—Г—О –њ–ї–Њ—В–љ–Њ—Б—В—М –њ–Њ —Б–Є—Б—В–µ–Љ–µ —Б–Њ–њ—А—П–ґ–µ–љ–Є—П –Њ—В —Б–µ–±—П (–њ–Њ–≤—Л—И–∞—О—В —Н–ї–µ–Ї—В—А–Њ–љ–љ—Г—О –њ–ї–Њ—В–љ–Њ—Б—В—М –≤ —Б–Њ–њ—А—П–ґ–µ–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ–µ). –Ъ –љ–Є–Љ –Њ—В–љ–Њ—Б—П—В—Б—П –≥—А—Г–њ–њ—Л, –Ї–Њ—В–Њ—А—Л–µ —Б–Њ–і–µ—А–ґ–∞—В –∞—В–Њ–Љ—Л —Б –љ–µ–њ–Њ–і–µ–ї–µ–љ–љ–Њ–є –њ–∞—А–Њ–є —Н–ї–µ–Ї—В—А–Њ–љ–Њ–≤, —Б–њ–Њ—Б–Њ–±–љ—Л–µ –Ї –њ–µ—А–µ–і–∞—З–µ —Н—В–Њ–є –њ–∞—А—Л —Н–ї–µ–Ї—В—А–Њ–љ–Њ–≤ –≤ –Њ–±—Й—Г—О —Б–Є—Б—В–µ–Љ—Г —Б–Њ–њ—А—П–ґ–µ–љ–Є—П.
–Ч–∞–Љ–µ—Б—В–Є—В–µ–ї–Є, –≤—Л–Ј—Л–≤–∞—О—Й–Є–µ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є –Љ–µ–Ј–Њ–Љ–µ—А–љ—Л–є —Н—Д—Д–µ–Ї—В (—Н–ї–µ–Ї—В—А–Њ–љ–Њ–і–Њ–љ–Њ—А—Л): ¬≠-NH2, ¬≠-OH.
–Э–∞–њ—А–Є–Љ–µ—А, –≤ –Љ–Њ–ї–µ–Ї—Г–ї–µ —Д–µ–љ–Њ–ї–∞ –°6–Э5–Ю–Э –≥—А—Г–њ–њ–∞ вАУ–Ю–Э –њ—А–Њ—П–≤–ї—П–µ—В +–Ь-—Н—Д—Д–µ–Ї—В –Ј–∞ —Б—З–µ—В —Г—З–∞—Б—В–Є—П –Њ–і–љ–Њ–є –Є–Ј –љ–µ–њ–Њ–і–µ–ї–µ–љ–љ—Л—Е —Н–ї–µ–Ї—В—А–Њ–љ–љ—Л—Е –њ–∞—А –∞—В–Њ–Љ–∞ –Ї–Є—Б–ї–Њ—А–Њ–і–∞ –≤ —Б–Є—Б—В–µ–Љ–µ —Б–Њ–њ—А—П–ґ–µ–љ–Є—П:
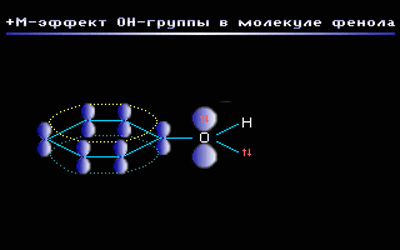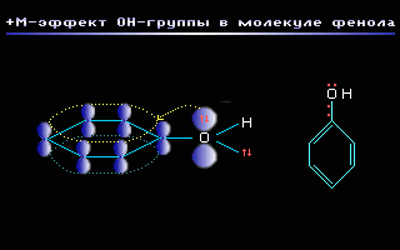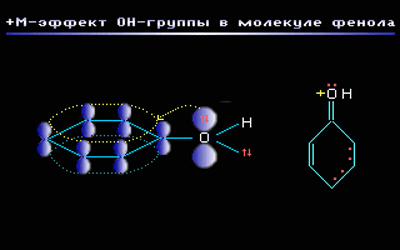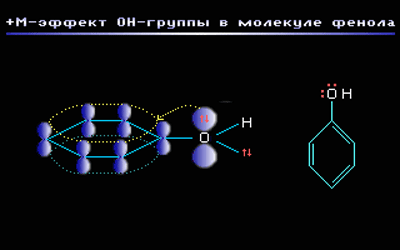
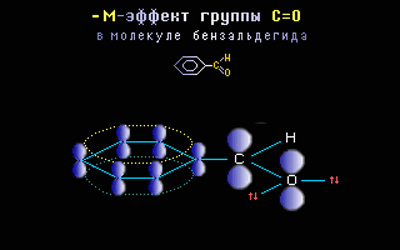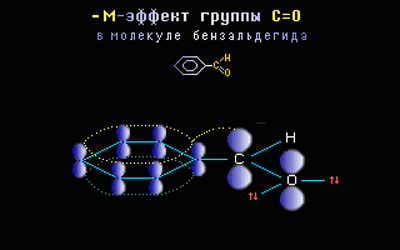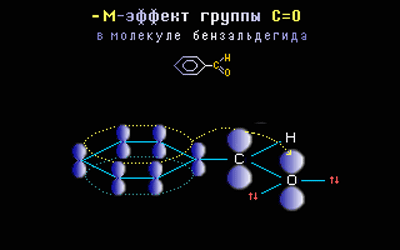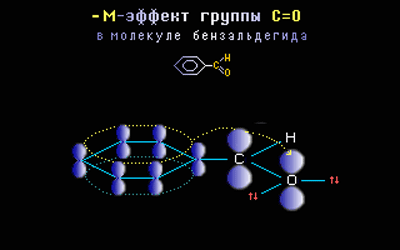
вАУ–Ь-—Н—Д—Д–µ–Ї—В –њ—А–Њ—П–≤–ї—П—О—В –Ј–∞–Љ–µ—Б—В–Є—В–µ–ї–Є —Б —Н–ї–µ–Ї—В—А–Њ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–Љ–Є –∞—В–Њ–Љ–∞–Љ–Є –Є —Б–Љ–µ—Й–∞—О—Й–Є–µ —Н–ї–µ–Ї—В—А–Њ–љ–љ—Г—О –њ–ї–Њ—В–љ–Њ—Б—В—М –љ–∞ —Б–µ–±—П (–њ–Њ–љ–Є–ґ–∞—О—В —Н–ї–µ–Ї—В—А–Њ–љ–љ—Г—О –њ–ї–Њ—В–љ–Њ—Б—В—М –≤ —Б–Њ–њ—А—П–ґ–µ–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ–µ).
–Ч–∞–Љ–µ—Б—В–Є—В–µ–ї–Є, –≤—Л–Ј—Л–≤–∞—О—Й–Є–µ –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–є –Љ–µ–Ј–Њ–Љ–µ—А–љ—Л–є —Н—Д—Д–µ–Ї—В (—Н–ї–µ–Ї—В—А–Њ–љ–Њ–∞–Ї—Ж–µ–њ—В–Њ—А—Л): –°–Э=–Ю, -NO2, ¬≠-COOH. –≠—В–Є –≥—А—Г–њ–њ—Л –Є–Љ–µ—О—В –љ–µ–њ–Њ–і–µ–ї–µ–љ–љ—Л–µ —Н–ї–µ–Ї—В—А–Њ–љ–љ—Л–µ –њ–∞—А—Л, –љ–Њ –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–µ–љ–љ–Њ–µ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–Є–µ –Њ—А–±–Є—В–∞–ї–µ–є —Б —Н—В–Є–Љ–Є —Н–ї–µ–Ї—В—А–Њ–љ–∞–Љ–Є –љ–µ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Є–Љ –≤—Б—В—Г–њ–∞—В—М –≤ —Б–Є—Б—В–µ–Љ—Г —Б–Њ–њ—А—П–ґ–µ–љ–Є—П. –Я–Њ—Н—В–Њ–Љ—Г, –≤ —Н—В–Њ–Љ —Б–ї—Г—З–∞–µ, –Ј–∞–Љ–µ—Б—В–Є—В–µ–ї—М –Њ—В—В—П–≥–Є–≤–∞–µ—В —Н–ї–µ–Ї—В—А–Њ–љ—Л –Є–Ј –Њ–±—Й–µ–є —Б–Є—Б—В–µ–Љ—Л —Б–Њ–њ—А—П–ґ–µ–љ–Є—П –Ј–∞ —Б—З–µ—В —Б–≤–Њ–µ–є –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Њ–є —Н–ї–µ–Ї—В—А–Њ–Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ—Б—В–Є.
–Э–∞–њ—А–Є–Љ–µ—А, ѕА-–Њ—А–±–Є—В–∞–ї—М –Ї—А–∞—В–љ–Њ–є —Б–≤—П–Ј–Є –°=–Ю –Є sp2-–Њ—А–±–Є—В–∞–ї–Є —Б –љ–µ–њ–Њ–і–µ–ї–µ–љ–љ—Л–Љ–Є –њ–∞—А–∞–Љ–Є —Н–ї–µ–Ї—В—А–Њ–љ–Њ–≤ –∞—В–Њ–Љ–∞ –Ї–Є—Б–ї–Њ—А–Њ–і–∞ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ—Л –њ–µ—А–њ–µ–љ–і–Є–Ї—Г–ї—П—А–љ–Њ –і—А—Г–≥ –і—А—Г–≥—Г, —В.–µ. –Є—Е –њ–µ—А–µ–Ї—А—Л–≤–∞–љ–Є–µ –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –Є –љ–Є –Њ–і–љ–∞ —Н–ї–µ–Ї—В—А–Њ–љ–љ–∞—П –њ–∞—А–∞ –Ї–Є—Б–ї–Њ—А–Њ–і–∞ –љ–µ –Љ–Њ–ґ–µ—В –њ–µ—А–µ–і–∞–≤–∞—В—М—Б—П –≤ ѕА-—Б–Є—Б—В–µ–Љ—Г:

 –†—Г–±—А–Є–Ї–Є:
–†—Г–±—А–Є–Ї–Є:  –Ґ–µ–≥–Є:
–Ґ–µ–≥–Є: 