–Р–ї–Ї–Є–љ—Л –≤–Њ –Љ–љ–Њ–≥–Є—Е —А–µ–∞–Ї—Ж–Є—П—Е –Њ–±–ї–∞–і–∞—О—В –±–Њ–ї—М—И–µ–є —А–µ–∞–Ї—Ж–Є–Њ–љ–љ–Њ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О, —З–µ–Љ –∞–ї–Ї–µ–љ—Л. –Ф–ї—П –∞–ї–Ї–Є–љ–Њ–≤, –Ї–∞–Ї –Є –і–ї—П –∞–ї–Ї–µ–љ–Њ–≤, —Е–∞—А–∞–Ї—В–µ—А–љ—Л —А–µ–∞–Ї—Ж–Є–Є –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є—П. –Ґ–∞–Ї –Ї–∞–Ї —В—А–Њ–є–љ–∞—П —Б–≤—П–Ј—М —Б–Њ–і–µ—А–ґ–Є—В –і–≤–µ ѕА-¬≠—Б–≤—П–Ј–Є, —А–µ–∞–Ї—Ж–Є–Є –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є—П –Ї –∞–ї–Ї–Є–љ–∞–Љ –Љ–Њ–≥—Г—В –њ—А–Њ–Є—Б—Е–Њ–і–Є—В—М –≤ –і–≤–µ —Б—В–∞–і–Є–Є.
–Т–љ–∞—З–∞–ї–µ –Є–і–µ—В –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –њ–Њ –Љ–µ—Б—В—Г –і–≤–Њ–є–љ–Њ–є ѕА-¬≠—Б–≤—П–Ј–Є —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л—Е –Њ–ї–µ—Д–Є–љ–Њ–≤, –∞ –Ј–∞—В–µ–Љ –њ–Њ –Љ–µ—Б—В—Г –≤—В–Њ—А–Њ–є ѕА-¬≠—Б–≤—П–Ј–Є —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л—Е –∞–ї–Ї–∞–љ–Њ–≤.
–†–µ–∞–Ї—Ж–Є–Є –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є—П –і–ї—П –∞–ї–Ї–Є–љ–Њ–≤ –њ—А–Њ—В–µ–Ї–∞—О—В –Љ–µ–і–ї–µ–љ–љ–µ–µ, —З–µ–Љ –і–ї—П –∞–ї–Ї–µ–љ–Њ–≤. –≠—В–Њ –Њ–±—К—П—Б–љ—П–µ—В—Б—П —В–µ–Љ, —З—В–Њ ѕА-¬≠—Н–ї–µ–Ї—В—А–Њ–љ–љ–∞—П –њ–ї–Њ—В–љ–Њ—Б—В—М —В—А–Њ–є–љ–Њ–є —Б–≤—П–Ј–Є —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–∞ –±–Њ–ї–µ–µ –Ї–Њ–Љ–њ–∞–Ї—В–љ–Њ, —З–µ–Љ –≤ –∞–ї–Ї–µ–љ–∞—Е, –Є –њ–Њ—Н—В–Њ–Љ—Г –Љ–µ–љ–µ–µ –і–Њ—Б—В—Г–њ–љ–∞ –і–ї—П –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є—П —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є —А–µ–∞–≥–µ–љ—В–∞–Љ–Є.
–†–µ–∞–Ї—Ж–Є–Є –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є—П
1. –У–Є–і—А–Є—А–Њ–≤–∞–љ–Є–µ
–Я—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –≤–Њ–і–Њ—А–Њ–і–∞ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –њ—А–Є –љ–∞–≥—А–µ–≤–∞–љ–Є–Є –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –Љ–µ—В–∞–ї–ї–Є—З–µ—Б–Ї–Є—Е –Ї–∞—В–∞–ї–Є–Ј–∞—В–Њ—А–Њ–≤. –†–µ–∞–Ї—Ж–Є—П –њ—А–Њ—В–µ–Ї–∞–µ—В –≤ –і–≤–µ —Б—В–∞–і–Є–Є: –∞–ї–Ї–Є–љ—Л –њ—А–Є—Б–Њ–µ–і–Є–љ—П—О—В –≤–Њ–і–Њ—А–Њ–і —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ –∞–ї–Ї–µ–љ–Њ–≤ (—А–∞–Ј—А—Л–≤–∞–µ—В—Б—П –њ–µ—А–≤–∞—П ѕА-¬≠—Б–≤—П–Ј—М), –∞ –Ј–∞—В–µ–Љ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ –∞–ї–Ї–∞–љ–Њ–≤ (—А–∞–Ј—А—Л–≤–∞–µ—В—Б—П –≤—В–Њ—А–∞—П ѕА-¬≠—Б–≤—П–Ј—М):

2. –У–∞–ї–Њ–≥–µ–љ–Є—А–Њ–≤–∞–љ–Є–µ
–Я—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –≥–∞–ї–Њ–≥–µ–љ–Њ–≤ –њ—А–Њ—В–µ–Ї–∞–µ—В —В–∞–Ї–ґ–µ –≤ –і–≤–µ —Б—В–∞–і–Є–Є. –Э–∞ –њ–µ—А–≤–Њ–є —Б—В–∞–і–Є–Є –Њ–±—А–∞–Ј—Г—О—В—Б—П –і–Є–≥–∞–ї–Њ–≥–µ–љ–∞–ї–Ї–µ–љ—Л, –љ–∞ –≤—В–Њ—А–Њ–є вАУ —В–µ—В—А–∞–≥–∞–ї–Њ–≥–µ–љ–∞–ї–Ї–∞–љ—Л:

–†–µ–∞–Ї—Ж–Є—П –∞–ї–Ї–Є–љ–Њ–≤ —Б –±—А–Њ–Љ–љ–Њ–є –≤–Њ–і–Њ–є —П–≤–ї—П–µ—В—Б—П –Ї–∞—З–µ—Б—В–≤–µ–љ–љ–Њ–є —А–µ–∞–Ї—Ж–Є–µ–є –љ–∞ –∞–ї–Ї–Є–љ—Л. –С—А–Њ–Љ–љ–∞—П –≤–Њ–і–∞ –Њ–±–µ—Б—Ж–≤–µ—З–Є–≤–∞–µ—В—Б—П.
–Т–Є–і–µ–Њ–Њ–њ—Л—В ¬Ђ–Т–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ –∞—Ж–µ—В–Є–ї–µ–љ–∞ —Б –±—А–Њ–Љ–љ–Њ–є –≤–Њ–і–Њ–є¬ї
–Т–Є–і–µ–Њ–Њ–њ—Л—В ¬Ђ–Т–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ –∞—Ж–µ—В–Є–ї–µ–љ–∞ —Б —Е–ї–Њ—А–Њ–Љ¬ї
3. –У–Є–і—А–Њ–≥–∞–ї–Њ–≥–µ–љ–Є—А–Њ–≤–∞–љ–Є–µ
–У–∞–ї–Њ–≥–µ–љ–Њ–≤–Њ–і–Њ—А–Њ–і—Л –њ—А–Є—Б–Њ–µ–і–Є–љ—П—О—В—Б—П –Ї –∞–ї–Ї–Є–љ–∞–Љ –≤ –і–≤–µ —Б—В–∞–і–Є–Є. –Т—В–Њ—А–∞—П —Б—В–∞–і–Є—П –Є–і–µ—В –њ–Њ –њ—А–∞–≤–Є–ї—Г –Ь–∞—А–Ї–Њ–≤–љ–Є–Ї–Њ–≤–∞. –Я—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –ЭCl –≤ –Њ—В—Б—Г—В—Б—В–≤–Є–Є –Ї–∞—В–∞–ї–Є–Ј–∞—В–Њ—А–∞ –Є–і–µ—В –Њ—З–µ–љ—М –Љ–µ–і–ї–µ–љ–љ–Њ. –Ъ–∞—В–∞–ї–Є–Ј–∞—В–Њ—А–Њ–Љ —Н—В–Њ–є —А–µ–∞–Ї—Ж–Є–Є —Б–ї—Г–ґ–∞—В –Ї–Є—Б–ї–Њ—В—Л –Ы—М—О–Є—Б–∞ вАУ —Б–Њ–ї–Є –Љ–µ–і–Є (I) –Є —А—В—Г—В–Є (II):

–Я–Њ–ї—Г—З–∞–µ–Љ—Л–є –њ—А–Њ–і—Г–Ї—В вАУ —Е–ї–Њ—А–Є—Б—В—Л–є –≤–Є–љ–Є–ї (–≤–Є–љ–Є–ї—Е–ї–Њ—А–Є–і) вАУ –њ–Њ–і–Њ–±–љ–Њ —Н—В–Є–ї–µ–љ—Г –ї–µ–≥–Ї–Њ –њ–Њ–ї–Є–Љ–µ—А–Є–Ј—Г–µ—В—Б—П, –Њ–±—А–∞–Ј—Г—П –њ–Њ–ї–Є–Љ–µ—А вАУ –њ–Њ–ї–Є–≤–Є–љ–Є–ї—Е–ї–Њ—А–Є–і, –Ї–Њ—В–Њ—А—Л–є —И–Є—А–Њ–Ї–Њ –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –≤ –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–µ –њ–Њ–ї–Є–≤–Є–љ–Є–ї—Е–ї–Њ—А–Є–і–љ—Л—Е —Б–Љ–Њ–ї:

4. –У–Є–і—А–∞—В–∞—Ж–Є—П (—А–µ–∞–Ї—Ж–Є—П –Ъ—Г—З–µ—А–Њ–≤–∞)
–Я—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –≤–Њ–і—Л –њ—А–Њ—В–µ–Ї–∞–µ—В –≤ –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є —Б–Њ–ї–µ–є —А—В—Г—В–Є (II) –њ—А–Є –љ–∞–≥—А–µ–≤–∞–љ–Є–Є вАУ HgSO4, Hg (NO3)2 вАУ —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ —Г–Ї—Б—Г—Б–љ–Њ–≥–Њ –∞–ї—М–і–µ–≥–Є–і–∞ (–њ—А–Є –Њ–±—Л—З–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е –∞—Ж–µ—В–Є–ї–µ–љ —Б –≤–Њ–і–Њ–є –љ–µ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤—Г–µ—В):

–Э–∞ –њ–µ—А–≤–Њ–є —Б—В–∞–і–Є–Є —А–µ–∞–Ї—Ж–Є–Є –Њ–±—А–∞–Ј—Г–µ—В—Б—П –љ–µ–њ—А–µ–і–µ–ї—М–љ—Л–є —Б–њ–Є—А—В, –≤ –Ї–Њ—В–Њ—А–Њ–Љ –≥–Є–і—А–Њ–Ї—Б–Є–ї—М–љ–∞—П –≥—А—Г–њ–њ–∞ –љ–∞—Е–Њ–і–Є—В—Б—П –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ —Г –∞—В–Њ–Љ–∞ —Г–≥–ї–µ—А–Њ–і–∞ –њ—А–Є –і–≤–Њ–є–љ–Њ–є —Б–≤—П–Ј–Є. –Ґ–∞–Ї–Є–µ —Б–њ–Є—А—В—Л –њ—А–Є–љ—П—В–Њ –љ–∞–Ј–≤–∞—В—М –≤–Є–љ–Є–ї–Њ–≤—Л–Љ–Є –Є–ї–Є –µ–љ–Њ–ї–∞–Љ–Є.
–Ю—В–ї–Є—З–Є—В–µ–ї—М–љ–Њ–є —З–µ—А—В–Њ–є –µ–љ–Њ–ї–Њ–≤ —П–≤–ї—П–µ—В—Б—П –Є—Е –љ–µ—Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М. –Т –Љ–Њ–Љ–µ–љ—В –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –Њ–љ–Є –Є–Ј–Њ–Љ–µ—А–Є–Ј—Г—О—В—Б—П –≤ –±–Њ–ї–µ–µ —Б—В–∞–±–Є–ї—М–љ—Л–µ –Ї–∞—А–±–Њ–љ–Є–ї—М–љ—Л–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П (–∞–ї—М–і–µ–≥–Є–і—Л –Є–ї–Є –Ї–µ—В–Њ–љ—Л) - –≤–Њ–і–Њ—А–Њ–і –≥–Є–і—А–Њ–Ї—Б–Є–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л –њ–µ—А–µ—Е–Њ–і–Є—В –Ї —Б–Њ—Б–µ–і–љ–µ–Љ—Г –∞—В–Њ–Љ—Г —Г–≥–ї–µ—А–Њ–і—Г. –Я—А–Є —Н—В–Њ–Љ ѕА¬≠-—Б–≤—П–Ј—М –Љ–µ–ґ–і—Г –∞—В–Њ–Љ–∞–Љ–Є —Г–≥–ї–µ—А–Њ–і–∞ —А–∞–Ј—А—Л–≤–∞–µ—В—Б—П –Є –Њ–±—А–∞–Ј—Г–µ—В—Б—П ѕА-¬≠—Б–≤—П–Ј—М –Љ–µ–ґ–і—Г –∞—В–Њ–Љ–Њ–Љ —Г–≥–ї–µ—А–Њ–і–∞ –Є –∞—В–Њ–Љ–Њ–Љ –Ї–Є—Б–ї–Њ—А–Њ–і–∞. –Я—А–Є—З–Є–љ–Њ–є –Є–Ј–Њ–Љ–µ—А–Є–Ј–∞—Ж–Є–Є —П–≤–ї—П–µ—В—Б—П –±–Њ–ї—М—И–∞—П –њ—А–Њ—З–љ–Њ—Б—В—М –і–≤–Њ–є–љ–Њ–є —Б–≤—П–Ј–Є –°=–Ю –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –і–≤–Њ–є–љ–Њ–є —Б–≤—П–Ј—М—О –°=–°.
–У–Є–і—А–∞—В–∞—Ж–Є—П –≥–Њ–Љ–Њ–ї–Њ–≥–Њ–≤ –∞—Ж–µ—В–Є–ї–µ–љ–∞ –њ—А–Њ—В–µ–Ї–∞–µ—В –њ–Њ –њ—А–∞–≤–Є–ї—Г –Ь–∞—А–Ї–Њ–≤–љ–Є–Ї–Њ–≤–∞, –Є –Њ–±—А–∞–Ј—Г—О—Й–Є–µ—Б—П –µ–љ–Њ–ї—Л –Є–Ј–Њ–Љ–µ—А–Є–Ј—Г—О—В—Б—П –≤ –Ї–µ—В–Њ–љ—Л:

5. –†–µ–∞–Ї—Ж–Є–Є –њ–Њ–ї–Є–Љ–µ—А–Є–Ј–∞—Ж–Є–Є
–Т –њ—А–Є—Б—Г—В—Б—В–≤–Є–Є –Ї–∞—В–∞–ї–Є–Ј–∞—В–Њ—А–Њ–≤ –∞–ї–Ї–Є–љ—Л –Љ–Њ–≥—Г—В —А–µ–∞–≥–Є—А–Њ–≤–∞—В—М –і—А—Г–≥ —Б –і—А—Г–≥–Њ–Љ, –њ—А–Є—З–µ–Љ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Г—Б–ї–Њ–≤–Є–є –Њ–±—А–∞–Ј—Г—О—В—Б—П —А–∞–Ј–ї–Є—З–љ—Л–µ –њ—А–Њ–і—Г–Ї—В—Л.
1.–Ф–Є–Љ–µ—А–Є–Ј–∞—Ж–Є—П –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –≤–Њ–і–љ–Њ-–∞–Љ–Љ–Є–∞—З–љ–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞ CuCl:

–Т–Є–љ–Є–ї–∞—Ж–µ—В–Є–ї–µ–љ –Њ–±–ї–∞–і–∞–µ—В –±–Њ–ї—М—И–Њ–є —А–µ–∞–Ї—Ж–Є–Њ–љ–љ–Њ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О вАУ –њ—А–Є—Б–Њ–µ–і–Є–љ—П—П —Е–ї–Њ—А–Њ–≤–Њ–і–Њ—А–Њ–і, –Њ–љ –Њ–±—А–∞–Ј—Г–µ—В —Е–ї–Њ—А–Њ–њ—А–µ–љ (2-—Е–ї–Њ—А–±—Г—В–∞–і–Є–µ–љ-1,3), –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л–є –і–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П –Є—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Е–ї–Њ—А–њ—А–µ–љ–Њ–≤–Њ–≥–Њ –Ї–∞—Г—З—Г–Ї–∞:

2.–Ґ—А–Є–Љ–µ—А–Є–Ј–∞—Ж–Є—П –∞—Ж–µ—В–Є–ї–µ–љ–∞ –љ–∞–і –∞–Ї—В–Є–≤–Є—А–Њ–≤–∞–љ–љ—Л–Љ —Г–≥–ї–µ–Љ –њ—А–Є–≤–Њ–і–Є—В –Ї –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О –±–µ–љ–Ј–Њ–ї–∞ (—А–µ–∞–Ї—Ж–Є—П –Ч–µ–ї–Є–љ—Б–Ї–Њ–≥–Њ):


–Т –∞–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є —В—А–Є–Љ–µ—А–Є–Ј–∞—Ж–Є–Є –Љ–Њ–≥—Г—В –≤—Б—В—Г–њ–∞—В—М —В–∞–Ї–ґ–µ –Є –±–ї–Є–ґ–∞–є—И–Є–µ –≥–Њ–Љ–Њ–ї–Њ–≥–Є –∞—Ж–µ—В–Є–ї–µ–љ–∞, –љ–∞–њ—А–Є–Љ–µ—А –њ—А–Њ–њ–Є–љ:

–†–µ–∞–Ї—Ж–Є–Є –Њ–Ї–Є—Б–ї–µ–љ–Є—П
1. –У–Њ—А–µ–љ–Є–µ
–Я—А–Є —Б–≥–Њ—А–∞–љ–Є–Є –∞–ї–Ї–Є–љ–Њ–≤ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –Є—Е –њ–Њ–ї–љ–Њ–µ –Њ–Ї–Є—Б–ї–µ–љ–Є–µ –і–Њ –°–Ю2 –Є –Э2–Ю. –У–Њ—А–µ–љ–Є–µ –∞—Ж–µ—В–Є–ї–µ–љ–∞ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –≤—Л–і–µ–ї–µ–љ–Є–µ–Љ –±–Њ–ї—М—И–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —В–µ–њ–ї–∞:
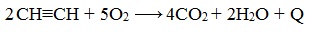
–Т–Є–і–µ–Њ–Њ–њ—Л—В ¬Ђ–У–Њ—А–µ–љ–Є–µ –∞—Ж–µ—В–Є–ї–µ–љ–∞¬ї
–Ґ–µ–Љ–њ–µ—А–∞—В—Г—А–∞ –∞—Ж–µ—В–Є–ї–µ–љ–Њ–≤–Њ-–Ї–Є—Б–ї–Њ—А–Њ–і–љ–Њ–≥–Њ –њ–ї–∞–Љ–µ–љ–Є –і–Њ—Б—В–Є–≥–∞–µ—В 2800- 3000¬∞–°. –Э–∞ —Н—В–Њ–Љ –Њ—Б–љ–Њ–≤–∞–љ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞—Ж–µ—В–Є–ї–µ–љ–∞ –і–ї—П —Б–≤–∞—А–Ї–Є –Є —А–µ–Ј–Ї–Є –Љ–µ—В–∞–ї–ї–∞. –Р—Ж–µ—В–Є–ї–µ–љ –Њ–±—А–∞–Ј—Г–µ—В —Б –≤–Њ–Ј–і—Г—Е–Њ–Љ –Є –Ї–Є—Б–ї–Њ—А–Њ–і–Њ–Љ –≤–Ј—А—Л–≤–Њ–Њ–њ–∞—Б–љ—Л–µ —Б–Љ–µ—Б–Є.
–Т–Є–і–µ–Њ–Њ–њ—Л—В ¬Ђ–Т–Ј—А—Л–≤ —Б–Љ–µ—Б–Є –∞—Ж–µ—В–Є–ї–µ–љ–∞ —Б –Ї–Є—Б–ї–Њ—А–Њ–і–Њ–Љ¬ї
–Т —Б–ґ–∞—В–Њ–Љ, –Є –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ —Б–ґ–Є–ґ–µ–љ–љ–Њ–Љ, —Б–Њ—Б—В–Њ—П–љ–Є–Є –Њ–љ —Б–њ–Њ—Б–Њ–±–µ–љ –≤–Ј—А—Л–≤–∞—В—М—Б—П –Њ—В —Г–і–∞—А–∞. –Я–Њ—Н—В–Њ–Љ—Г –∞—Ж–µ—В–Є–ї–µ–љ —Е—А–∞–љ–Є—В—Б—П –≤ —Б—В–∞–ї—М–љ—Л—Е –±–∞–ї–ї–Њ–љ–∞—Е –≤ –≤–Є–і–µ —А–∞—Б—В–≤–Њ—А–Њ–≤ –≤ –∞—Ж–µ—В–Њ–љ–µ, –Ї–Њ—В–Њ—А—Л–Љ –њ—А–Њ–њ–Є—В—Л–≤–∞—О—В –∞—Б–±–µ—Б—В.
2. –Э–µ–њ–Њ–ї–љ–Њ–µ –Њ–Ї–Є—Б–ї–µ–љ–Є–µ
–Р—Ж–µ—В–Є–ї–µ–љ –Є –µ–≥–Њ –≥–Њ–Љ–Њ–ї–Њ–≥–Є –ї–µ–≥–Ї–Њ –Њ–Ї–Є—Б–ї—П—О—В—Б—П –Њ–Ї–Є—Б–ї–Є—В–µ–ї—П–Љ–Є — –ЪMnO4, K2Cr2O7. –Р–ї–Ї–Є–љ—Л –Њ–Ї–Є—Б–ї—П—О—В—Б—П —Б —А–∞–Ј—А—Л–≤–Њ–Љ –Љ–Њ–ї–µ–Ї—Г–ї—Л –њ–Њ —В—А–Њ–є–љ–Њ–є —Б–≤—П–Ј–Є. –°—В—А–Њ–µ–љ–Є–µ –њ—А–Њ–і—Г–Ї—В–Њ–≤ –Њ–Ї–Є—Б–ї–µ–љ–Є—П –Ј–∞–≤–Є—Б–Є—В –Њ—В –њ—А–Є—А–Њ–і—Л –Њ–Ї–Є—Б–ї–Є—В–µ–ї—П –Є —Г—Б–ї–Њ–≤–Є–є –њ—А–Њ–≤–µ–і–µ–љ–Є—П —А–µ–∞–Ї—Ж–Є–є.
–Р–ї–Ї–Є–љ—Л –Њ–±–µ—Б—Ж–≤–µ—З–Є–≤–∞—О—В —А–∞–Ј–±–∞–≤–ї–µ–љ–љ—Л–є —А–∞—Б—В–≤–Њ—А –њ–µ—А–Љ–∞–љ–≥–∞–љ–∞—В–∞ –Ї–∞–ї–Є—П, —З—В–Њ –і–Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Є—Е –љ–µ–љ–∞—Б—Л—Й–µ–љ–љ–Њ—Б—В—М.
–∞) –Љ—П–≥–Ї–Њ–µ –Њ–Ї–Є—Б–ї–µ–љ–Є–µ
–Ь—П–≥–Ї–Њ–µ –Њ–Ї–Є—Б–ї–µ–љ–Є–µ –∞–ї–Ї–Є–љ–Њ–≤ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –±–µ–Ј —А–∞–Ј—А—Л–≤–∞ ѕГ-—Б–≤—П–Ј–Є –°вФА–° (—А–∞–Ј—А—Г—И–∞—О—В—Б—П —В–Њ–ї—М–Ї–Њ ѕА-¬≠—Б–≤—П–Ј–Є).
–Э–∞–њ—А–Є–Љ–µ—А, –њ—А–Є –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–Є –∞—Ж–µ—В–Є–ї–µ–љ–∞ —Б —А–∞–Ј–±–∞–≤–ї–µ–љ–љ—Л–Љ —А–∞—Б—В–≤–Њ—А–Њ–Љ –ЪMnO4 –њ—А–Є –Ї–Њ–Љ–љ–∞—В–љ–Њ–є —В–µ–Љ–њ–µ—А–∞—В—Г—А–µ –Њ–±—А–∞–Ј—Г–µ—В—Б—П –і–≤—Г—Е–Њ—Б–љ–Њ–≤–љ–∞—П —Й–∞–≤–µ–ї–µ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞:

–Т –љ–µ–є—В—А–∞–ї—М–љ–Њ–є –Є —Б–ї–∞–±–Њ—Й–µ–ї–Њ—З–љ–Њ–є —Б—А–µ–і–∞—Е –љ–∞ —Е–Њ–ї–Њ–і–µ –Њ–±—А–∞–Ј—Г—О—В—Б—П —Б–Њ–ї–Є –Ї–∞—А–±–Њ–љ–Њ–≤—Л—Е –Ї–Є—Б–ї–Њ—В. –Я—А–Є –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–Є –∞—Ж–µ—В–Є–ї–µ–љ–∞ —Б –≤–Њ–і–љ—Л–Љ —А–∞—Б—В–≤–Њ—А–Њ–Љ –њ–µ—А–Љ–∞–љ–≥–∞–љ–∞—В–∞ –Ї–∞–ї–Є—П –Њ–±—А–∞–Ј—Г–µ—В—Б—П —Б–Њ–ї—М —Й–∞–≤–µ–ї–µ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л (–Њ–Ї—Б–∞–ї–∞—В –Ї–∞–ї–Є—П):

–±) –Ц–µ—Б—В–Ї–Њ–µ –Њ–Ї–Є—Б–ї–µ–љ–Є–µ
–Я—А–Є –ґ–µ—Б—В–Ї–Њ–Љ –Њ–Ї–Є—Б–ї–µ–љ–Є–Є (–љ–∞–≥—А–µ–≤–∞–љ–Є–µ, –Ї–Њ–љ—Ж–µ–љ—В—А–Є—А–Њ–≤–∞–љ–љ—Л–µ —А–∞—Б—В–≤–Њ—А—Л, –Ї–Є—Б–ї–∞—П —Б—А–µ–і–∞) –њ—А–Њ–Є—Б—Е–Њ–і–Є—В —А–∞—Б—Й–µ–њ–ї–µ–љ–Є–µ —Г–≥–ї–µ—А–Њ–і–љ–Њ–≥–Њ —Б–Ї–µ–ї–µ—В–∞ –Љ–Њ–ї–µ–Ї—Г–ї—Л –∞–ї–Ї–Є–љ–∞ –њ–Њ —В—А–Њ–є–љ–Њ–є —Б–≤—П–Ј–Є –Є –Њ–±—А–∞–Ј—Г—О—В—Б—П –Ї–∞—А–±–Њ–љ–Њ–≤—Л–µ –Ї–Є—Б–ї–Њ—В—Л.
–Ю–Ї–Є—Б–ї–µ–љ–Є–µ –∞–ї–Ї–Є–љ–Њ–≤ –њ–µ—А–Љ–∞–љ–≥–∞–љ–∞—В–Њ–Љ –Ї–∞–ї–Є—П –≤ –Ї–Є—Б–ї–Њ–є —Б—А–µ–і–µ –њ—А–Є –љ–∞–≥—А–µ–≤–∞–љ–Є–Є —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —А–∞–Ј—А—Л–≤–Њ–Љ —Г–≥–ї–µ—А–Њ–і–љ–Њ–є —Ж–µ–њ–Є –њ–Њ –Љ–µ—Б—В—Г —В—А–Њ–є–љ–Њ–є —Б–≤—П–Ј–Є –Є –њ—А–Є–≤–Њ–і–Є—В –Ї –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –Ї–∞—А–±–Њ–љ–Њ–≤—Л—Е –Ї–Є—Б–ї–Њ—В:

–Ю–Ї–Є—Б–ї–µ–љ–Є–µ –∞–ї–Ї–Є–љ–Њ–≤, —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е —В—А–Њ–є–љ—Г—О —Б–≤—П–Ј—М —Г –Ї—А–∞–є–љ–µ–≥–Њ –∞—В–Њ–Љ–∞ —Г–≥–ї–µ—А–Њ–і–∞, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –≤ —Н—В–Є—Е –ґ–µ —Г—Б–ї–Њ–≤–Є—П—Е –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ –Ї–∞—А–±–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –Є –≤—Л–і–µ–ї–µ–љ–Є–µ–Љ —Г–≥–ї–µ–Ї–Є—Б–ї–Њ–≥–Њ –≥–∞–Ј–∞:

–Т –Ї–Є—Б–ї–Њ–є —Б—А–µ–і–µ –Њ–Ї–Є—Б–ї–µ–љ–Є–µ –∞—Ж–µ—В–Є–ї–µ–љ–∞ –Є–і–µ—В –і–Њ —Й–∞–≤–µ–ї–µ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –Є–ї–Є —Г–≥–ї–µ–Ї–Є—Б–ї–Њ–≥–Њ –≥–∞–Ј–∞:

–Т–Є–і–µ–Њ–Њ–њ—Л—В ¬Ђ–Т–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ –∞—Ж–µ—В–Є–ї–µ–љ–∞ —Б —А–∞—Б—В–≤–Њ—А–Њ–Љ –њ–µ—А–Љ–∞–љ–≥–∞–љ–∞—В–∞ –Ї–∞–ї–Є—П¬ї
–†–µ–∞–Ї—Ж–Є—П –ЪMnO4 —П–≤–ї—П–µ—В—Б—П –Ї–∞—З–µ—Б—В–≤–µ–љ–љ–Њ–є —А–µ–∞–Ї—Ж–Є–µ–є –љ–∞ –∞–ї–Ї–Є–љ—Л. –†–∞—Б—В–≤–Њ—А –њ–µ—А–Љ–∞–љ–≥–∞–љ–∞—В–∞ –Ї–∞–ї–Є—П –Њ–±–µ—Б—Ж–≤–µ—З–Є–≤–∞–µ—В—Б—П.
–Ю–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ —Б–Њ–ї–µ–є
–Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В—М—О –∞–ї–Ї–Є–љ–Њ–≤, –Є–Љ–µ—О—Й–Є—Е –Ї–Њ–љ—Ж–µ–≤—Г—О —В—А–Њ–є–љ—Г—О —Б–≤—П–Ј—М (–∞–ї–Ї–Є–љ—Л-1), —П–≤–ї—П–µ—В—Б—П –Є—Е —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –њ—А–Њ—П–≤–ї—П—В—М —Б–ї–∞–±—Л–µ –Ї–Є—Б–ї–Њ—В–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞.
–Р—В–Њ–Љ—Л –≤–Њ–і–Њ—А–Њ–і–∞, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б sp-–≥–Є–±—А–Є–і–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–Љ–Є –∞—В–Њ–Љ–∞–Љ–Є —Г–≥–ї–µ—А–Њ–і–∞ –≤ –Љ–Њ–ї–µ–Ї—Г–ї–∞—Е –∞–ї–Ї–Є–љ–Њ–≤, –Њ–±–ї–∞–і–∞—О—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є –њ–Њ–і–≤–Є–ґ–љ–Њ—Б—В—М—О, —З—В–Њ –Њ–±—К—П—Б–љ—П–µ—В—Б—П –њ–Њ–ї—П—А–Є–Ј–∞—Ж–Є–µ–є ѕГ-—Б–≤—П–Ј–Є вЙ°–°вФА–Э. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –∞—В–Њ–Љ—Л –≤–Њ–і–Њ—А–Њ–і–∞ –Љ–Њ–≥—Г—В –Ј–∞–Љ–µ—Й–∞—В—М—Б—П –∞—В–Њ–Љ–∞–Љ–Є –Љ–µ—В–∞–ї–ї–Њ–≤, –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —З–µ–≥–Њ –Њ–±—А–∞–Ј—Г—О—В—Б—П —Б–Њ–ї–Є — –∞—Ж–µ—В–Є–ї–µ–љ–Є–і—Л.

–Р—Ж–µ—В–Є–ї–µ–љ–Є–і—Л —Й–µ–ї–Њ—З–љ—Л—Е –Є —Й–µ–ї–Њ—З–љ–Њ–Ј–µ–Љ–µ–ї—М–љ—Л—Е –Љ–µ—В–∞–ї–ї–Њ–≤ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –і–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П –≥–Њ–Љ–Њ–ї–Њ–≥–Њ–≤ –∞—Ж–µ—В–Є–ї–µ–љ–∞.
–Р—Ж–µ—В–Є–ї–µ–љ–Є–і—Л —Б–µ—А–µ–±—А–∞ –Є –Љ–µ–і–Є (I) –ї–µ–≥–Ї–Њ –Њ–±—А–∞–Ј—Г—О—В—Б—П –Є –≤—Л–њ–∞–і–∞—О—В –≤ –Њ—Б–∞–і–Њ–Ї –њ—А–Є –њ—А–Њ–њ—Г—Б–Ї–∞–љ–Є–Є –∞—Ж–µ—В–Є–ї–µ–љ–∞ —З–µ—А–µ–Ј –∞–Љ–Љ–Є–∞—З–љ—Л–є —А–∞—Б—В–≤–Њ—А –Њ–Ї—Б–Є–і–∞ —Б–µ—А–µ–±—А–∞ –Є–ї–Є —Е–ї–Њ—А–Є–і–∞ –Љ–µ–і–Є (I).

–Ю–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ —Б–µ—А–Њ–≤–∞—В–Њ- –±–µ–ї–Њ–≥–Њ –Њ—Б–∞–і–Ї–∞ –∞—Ж–µ—В–Є–ї–µ–љ–Є–і–∞ —Б–µ—А–µ–±—А–∞ (–Є–ї–Є –Ї—А–∞—Б–љ–Њ-–Ї–Њ—А–Є—З–љ–µ–≤–Њ–≥–Њ вАУ –∞—Ж–µ—В–Є–ї–µ–љ–Є–і–∞ –Љ–µ–і–Є) —Б–ї—Г–ґ–Є—В –Ї–∞—З–µ—Б—В–≤–µ–љ–љ–Њ–є —А–µ–∞–Ї—Ж–Є–µ–є –љ–∞ –Ї–Њ–љ—Ж–µ–≤—Г—О —В—А–Њ–є–љ—Г—О —Б–≤—П–Ј—М.
–Т–Є–і–µ–Њ–Њ–њ—Л—В ¬Ђ–Я–Њ–ї—Г—З–µ–љ–Є–µ –∞—Ж–µ—В–Є–ї–µ–љ–Є–і–∞ —Б–µ—А–µ–±—А–∞¬ї
–Т–Є–і–µ–Њ–Њ–њ—Л—В ¬Ђ–Я–Њ–ї—Г—З–µ–љ–Є–µ –∞—Ж–µ—В–Є–ї–µ–љ–Є–і–∞ –Љ–µ–і–Є¬ї
–Р—Ж–µ—В–Є–ї–µ–љ–Є–і—Л —Б–µ—А–µ–±—А–∞ –Є –Љ–µ–і–Є –Ї–∞–Ї —Б–Њ–ї–Є —Б–ї–∞–±—Л—Е –Њ—З–µ–љ—М –Ї–Є—Б–ї–Њ—В –ї–µ–≥–Ї–Њ —А–∞–Ј–ї–∞–≥–∞—О—В—Б—П –њ—А–Є –і–µ–є—Б—В–≤–Є–Є —Е–ї–Њ—А–Њ–≤–Њ–і–Њ—А–Њ–і–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л —Б –≤—Л–і–µ–ї–µ–љ–Є–µ–Љ –Є—Б—Е–Њ–і–љ–Њ–≥–Њ –∞–ї–Ї–Є–љ–∞.

–Р—Ж–µ—В–Є–ї–Є–љ–Є–і—Л —Б–µ—А–µ–±—А–∞ –Є –Љ–µ–і–Є –≤ —Б—Г—Е–Њ–Љ –≤–Є–і–µ –≤–Ј—А—Л–≤–∞—О—В—Б—П –Њ—В —Г–і–∞—А–∞. –Ю–і–љ–∞–Ї–Њ –Ї–∞—А–±–Є–і –Ї–∞–ї—М—Ж–Є—П, –Ї–Њ—В–Њ—А—Л–є —В–∞–Ї–ґ–µ —П–≤–ї—П–µ—В—Б—П –∞—Ж–µ—В–Є–ї–µ–љ–Є–і–Њ–Љ, –Њ—З–µ–љ—М —Г—Б—В–Њ–є—З–Є–≤ –Ї —Г–і–∞—А—Г. –Ю–љ —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В—Б—П –і–ї—П –њ–Њ–ї—Г—З–µ–љ–Є—П –∞—Ж–µ—В–Є–ї–µ–љ–∞.
–Т–Є–і–µ–Њ–Њ–њ—Л—В ¬Ђ–Э–µ—Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –∞—Ж–µ—В–Є–ї–µ–љ–Є–і–Њ–≤¬ї
–Х—Б–ї–Є —В—А–Њ–є–љ–∞—П —Б–≤—П–Ј—М –љ–∞—Е–Њ–і–Є—В—Б—П –љ–µ –љ–∞ –Ї–Њ–љ—Ж–µ —Ж–µ–њ–Є, —В–Њ –Ї–Є—Б–ї–Њ—В–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞ –Њ—В—Б—Г—В—Б—В–≤—Г—О—В (–љ–µ—В –њ–Њ–і–≤–Є–ґ–љ–Њ–≥–Њ –∞—В–Њ–Љ–∞ –≤–Њ–і–Њ—А–Њ–і–∞) –Є –∞—Ж–µ—В–Є–ї–µ–љ–Є–і—Л –љ–µ –Њ–±—А–∞–Ј—Г—О—В—Б—П.

–Р–ї–Ї–Є–љ—Л (–∞—Ж–µ—В–Є–ї–µ–љ–Њ–≤—Л–µ —Г–≥–ї–µ–≤–Њ–і–Њ—А–Њ–і—Л)

 –†—Г–±—А–Є–Ї–Є:
–†—Г–±—А–Є–Ї–Є:  –Ґ–µ–≥–Є:
–Ґ–µ–≥–Є: 